V léčbě metastatického kastračně rezistentního karcinomu prostaty máme k dispozici několik různých typů systémové léčby. Čím více linií terapie použijeme, tím více lze prodloužit život pacientů. I přes podanou léčbu, ale postupně u pacientů dochází k progresi onemocnění. Hledají se proto další postupy, které by prodloužily jejich přežití. PARP (poly(ADP-ribóza)polymeráza) inhibitory prokázaly u těchto pacientů účinnost jednak v monoterapii, jednak v kombinaci s ARTA (léčbou látkami cílenými na androgenní receptory – abirateron, enzalutamid). Nejzralejší data máme dosud k dispozici s PARPi olaparibem.
Zhoubné nádory prostaty patří mezi nejčastější onkologická onemocnění u mužů s incidencí v roce 2023 172,8/100 000. Přibližně 15 % nových případů se diagnostikuje v metastatickém stadiu (synchronní de novo postižení), další nemocní do tohoto stadia dospějí z původně lokalizovaného onemocnění (metachronní postižení). Nejčastějším místem metastatického postižení jsou skelet a lymfatické uzliny, méně často se vyskytují viscerální metastázy.
Metastatický karcinom prostaty je zpočátku hormonálně senzitivní onemocnění (mHSPC – metastatický hormon senzitivní karcinom). I přes uvedenou hormonální senzitivitu, dochází postupně k poklesu citlivosti na primární hormonální léčbu (androgen deprivační terapie – ADT), která se projeví elevací PSA, klinickou či radiologickou progresí. Onemocnění pak definujeme jako metastatický kastračně rezistentní karcinom prostaty (mCRPC).
Léčebné přístupy k mCRPC
Standardem léčby mCRPC byla od roku 2004 chemoterapie založená na podání docetaxelu. Následně došlo k významnému rozšíření léčebných možností v oblasti chemoterapie (kabazitaxel), vývoji nových radiofarmak (radium 223, lutecium 177) a léčby cílené na androgenní receptor (androgen receptor targeted therapy – ARTA). Z výčtu léčebných možností je zřejmé, že pacientům s mCRPC můžeme nabídnout několik linií léčby. Je prokázanou skutečnosti, že nemocní, kteří absolvují větší počet linií, mají delší celkové přežití (OS). Stanovení optimální sekvence léčby mCRPC v klinické praxi komplikuje absence využitelných prediktivních biomarkerů. V praxi proto musíme vycházet hlavně z klinických parametrů: výkonnostní stav, přítomnost komorbidit, symptomatologie onemocnění, lokalizace metastáz (kostní vs. viscerální). Neméně důležité je brát v úvahu i potenciální toxicitu terapie.
I přes skutečnost, že výše zmíněné léčebné postupy významně prodloužily přežití bez známek progrese (PFS) a OS, u velké většiny dochází postupně k další progresi onemocnění. Otázka zlepšení výsledků je proto nadále aktuální. Jednou z možností je zavedení nových skupin léků do léčebného algoritmu mCRPC, případně jejich kombinace s již stávajícími látkami. Mezi novější molekuly patří takzvané PARP (poly(ADP-ribóza)polymeráza) inhibitory (PARPi). Mechanismus účinku PARP inhibitorů spočívá v inhibici enzymů, které opravují poškozenou DNA. Mutace v genech opravujících DNA se vyskytují u karcinomu prostaty v 11–33 %, nejčastěji je zastoupena mutace v genu BRCA2. První publikované práce hodnotily PARPi olaparib.
Olaparib v monoterapii mCRPC
Olaparib je účinný inhibitor skupiny enzymů PARP1-3. Prokázal účinek u řady maligních onemocnění, dosud byly v ČR doménou použití diagnózy karcinomu ovaria či prsů. Většinou je vyžadováno stanovení germinální nebo somatické BRCA mutace. Olaparib byl hodnocen i v léčbě pokročilého karcinomu prostaty.
V roce 2020 byly publikovány výsledky klinické studie III. fáze PROfound, která hodnotila účinek olaparibu u pacientů s mCRPC po předchozí ARTA. Nemocní museli mít alteraci genů podílejících se přímo nebo nepřímo na opravě DNA pomocí mechanismu homologní rekombinace (HRR). Kohorta A měla 245 pacientů s alterací genů BRCA1, BRCA2 a ATM, nebo byly změny v dalších genech (kohorta B – 142 pacientů). Pacienti byli randomizování v poměru 2 : 1 k podání olaparibu, nebo dosud nepoužitou ARTA (abirateron nebo enzalutamid). Primárním cílem bylo zhodnotit přežití bez známek progrese pomocí zobrazovacích vyšetření (ibPFS) v kohortě pacientů A. Podání olaparibu významně prodloužilo v této kohortě ibPFS (7,4 vs. 3,6 měsíce; HR 0,34, 95% CI 0,25–0,47) i OS (18,5 vs 15,1 měsíce; HR 0,64, 95% CI 0,43–0,97). Podobně podání olaparibu mělo významný vliv i v rámci hodnocení dalších cílů klinické studie jako vyšší počet celkové léčebné odpovědi či prodloužení doby do objevení bolesti. Mediány ibPFS a OS byly významně prodlouženy u pacientů léčených olaparibem i v rámci celé populace (kohorta A + B dohromady). V podkupinové analýze byl prokázán benefit olaparibu na prodloužení OS i ibPFS bez ohledu na věk, lokalizaci metastatického postižení, předchozího podání chemoterapie, vstupní hodnoty PSA. Největší přínos olaparibu v kohortě A byl prokázán u pacientů s BRCA2 mutací. U pacientů léčených olaparibem se vyskytla toxicita stupně 3–4 u 51 % pacientů, dominoval výskyt anémie (21 %). Mezi další projevy léčby olaparibem patřila nevolnost, zvracení, průjem, únava, pokles hmotnosti a jiné. U 11 pacientů byla popsána plicní embolie. Kritika studie se může týkat skutečnosti, že u pacientů v kontrolním ramenu může existovat zkřížená rezistence sekvence ARTA–ARTA.
Olaparib v kombinační léčbě mCRPC
Preklinické modely potvrdily protinádorový účinek kombinace PARPi + ARTA. Možným mechanismem účinků zmíněné kombinace je pozitivní koregulace signalizace pomocí androgenního receptoru (AR) nebo inhibice transkripce genů podílejících se na homologní rekombinaci. Dalším účinkem působení může být vliv negenetických mechanismů na zvýšení senzitivity k PARPi.
V roce 2022 byly publikovány výsledky klinické studie III. fáze PROpel, která hodnotila kombinaci olaparib + abirateron. Kontrolním ramenem byl abirateron + placebo. Studijní populace představovala nemocné dosud neléčené pro mCRPC, pacienti mohli být předléčeni docetaxelem v rámci mHSPC. Celkem bylo hodnoceno 796 pacientů, randomizace v poměru 1 : 1. Primárním cílem bylo stanovit ibPFS. Mezi stratifikační faktory studie patřilo podání předchozí chemoterapie a lokalizace metastatického postižen (kostní vs. viscerální vs. jiné). Do klinické studie byli zahrnutí nemocní s převážně vyšším Gleasonovým skóre (GS 8–10 u dvou třetin nemocných). Prevalence mutace BRCA1byla 2,3 %, BRCA2 9,5 %. Charakteristika pacientů je uvedena v tabulce 1.
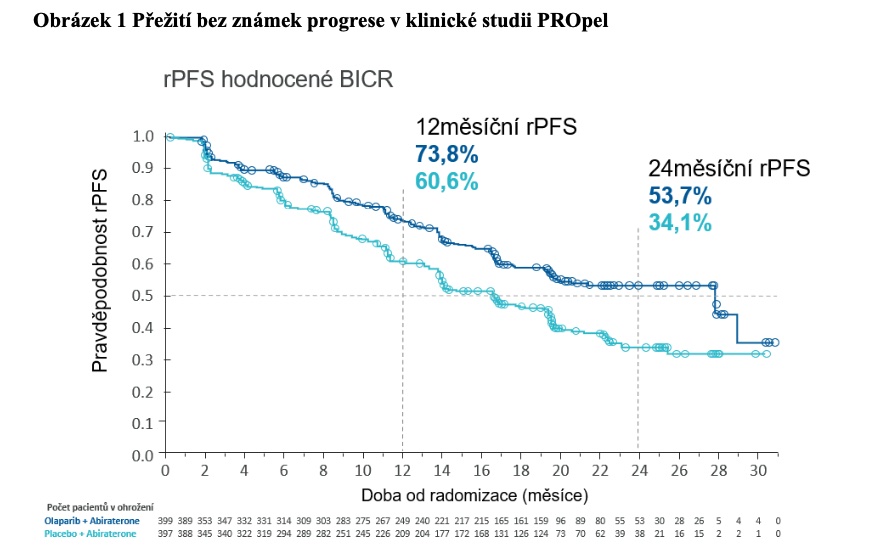
Kombinace olaparibu a abirateronu významně prodloužila medián ibPFS (obrázek 1) jak při vyhodnocení investigátory (24,4 vs. 16,6 měsíce; HR 0,66, 95% CI 0,54–0,81), tak i při zpracování nezávislými hodnotiteli (27,6 vs. 16,4 měsíce; HR 0,61, 95% CI 0,49–0,74).
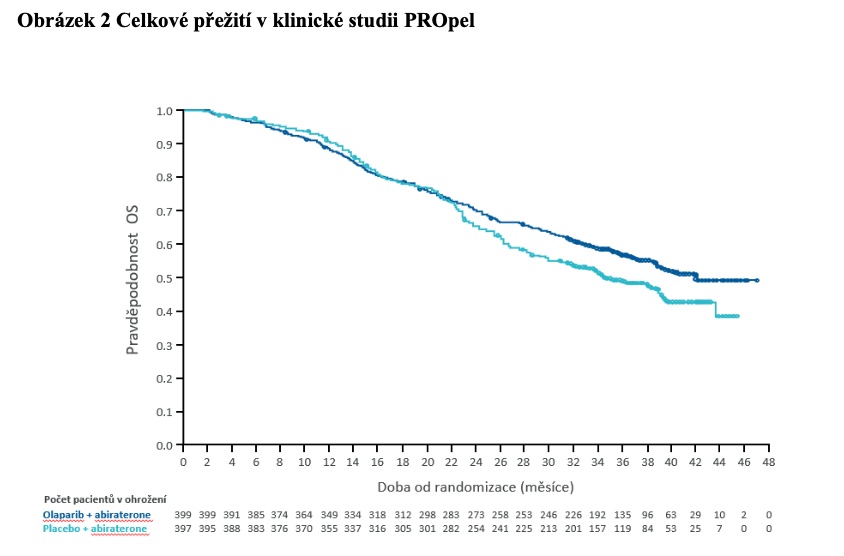
Benefit kombinace olaparib + abirateron na prodloužení ibPFS byl prokázán bez ohledu na věk, celkový PS (0 vs. 1), předchozí aplikaci docetaxelu, lokalizaci metastáz či přítomnost genetických mutací genů podílejících se na homologní rekombinaci. Data ohledně OS byla prezentována na ASCO GU 2023. Kombinace olaparib + abirateron demonstrovala trend k významnému prodloužení OS ve srovnání s kombinací abirateron + placebo (42,1 vs. 34,7 měsíce, HR 0,81, 95% CI 0,8–1,00) (obrázek 2).
Medián OS nad 3,5 roku v případě mCRPC je jedním z milníků moderní léčby tohoto onemocnění. Data byla posléze i publikována.
Explorativní post hoc analýza studie PROpel hodnotila vliv uvedené kombinace olaparib + abirateron u pacientů s přítomností mutace BRCA. Jednalo se celkem o 85 nemocných. V této skupině byl přínos kombinace jednoznačně prokázán jak v rPFS (HR 0,24, 95% CI 0,12–0,45), tak i v OS (HR 0,3, 95% CI 0,15–0,59). Efekt u pacientů bez BRCAmutací byl méně výrazný. V hodnocení rPFS bylo HR 0,77 (95% CI 0,63–0,96), při hodnocení OS již statisticky přínos kombinace nebyl zjištěn (HR 0,92, 95% CI 0,74–1,14).
Jiná recentně publikovaná analýza hodnotila význam kombinované léčby v podskupinách pacientů asymptomatických/mírně symptomatických vs. symptomatických. Stratifikace byla podle BPI-SF (Brief Pain Inventroy-Short Form) a nutnosti užívání opiátů. Celkem 560 pacientů bylo zařazeno do skupiny asymptomatických / mírně symptomatických, 183 nemocných bylo klasifikováno se symptomatickým onemocněním. Medián rPFS u pacientů asymptotických / mírně symptomatických byl významně prodloužen při kombinaci olaparib + abirateron (HR 0,59, 95% CI 0,46–0,76), podobně i medián OS (HR 0,77, 95% CI 0,59–1,00). Ve skupině symptomatických pacientů významné prodloužení rPFS (HR 0,78, 95% CI 0,54–1,13) ani OS (HR 0,82, 95% CI 0,58–1,16) nebylo pozorováno. Další hodnocení na podkladě přítomnosti mutaci HRR v obou skupinách nebylo provedeno.
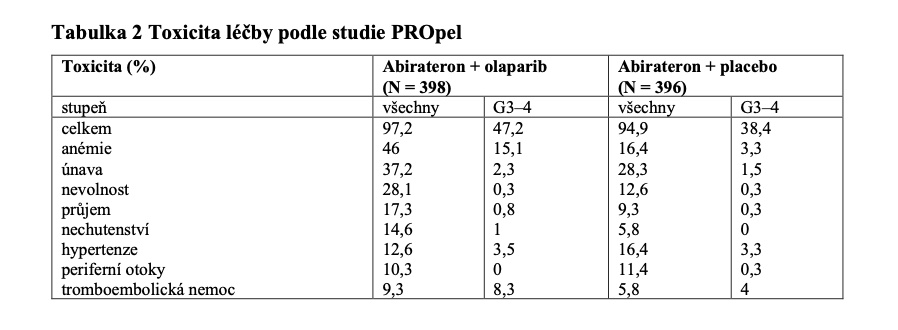
Při kombinované léčbě má důležitou roli i otázka, zda nedochází k dramatickému navýšení nežádoucích účinků. Nejčastějším projevem toxicity G3–4 u pacientů léčených kombinací byla anémie (15,1 vs. 3,3 %). Redukce olaparibu z důvodu tolerance byla popsána u 20,1 %, přerušení u 44,7 % a definitivní ukončení podávání olaparibu bylo u 13,8 % pacientů. Přehled toxicity je uveden v tabulce 2.
Závěr
Léčba mCRPC dosáhla za poslední roky významných pokroků. U pacientů se významně etablovala ARTA, která představuje nejčastější používanou modalitu u těch s pokročilým karcinomem prostaty. Výhodou ARTA je přijatelná tolerance, nicméně časem u většiny pacientů dojde k progresi onemocnění. Možností, jak prodloužit dobu do progrese, je kombinace ARTA s PARPi. Kombinace olaparib + abirateron prokázala významné prodloužení rPFS a OS. Je proto otázkou, pro jakou skupinu pacientů bude kombinace ARTA + PARPi optimální volbou. Na podkladě dat se zdá, že přínos bude mít kombinace hlavně u pacientů s BRCA1, 2 mutací. Větší profit budou mít dále pacienti asymptomatičtí / mírně symptomatičtí podle explorativních analýz registrační studie. Toto je i v souladu s úhradou v ČR, podle které je olaparib hrazen v kombinaci s abirateronem v prvoliniové léčbě u asymptomatických či mírně symptomatických pacientů s prokázanou poruchou reparace DNA (dHRR) a se stavem výkonnosti podle ECOG 0–1, u nichž chemoterapie není klinicky indikována.
Literatura u autorů, zdroj obrázků a tabulek – archiv autorů

•



